|
研究概要
1.高分子材料と血液適合性
これまで多くの血液適合性材料表面が研究されている。これを大雑把に分類すると①ミクロ相分離表面、 ②超親水性(散漫構造)表面、 ③生体膜類似表面、 ③生理活性物質固定化表面となる。これらの材料がその適合性を発現する理由として④を除いてはこれまで種々の考えが提案されてきているが、いずれも定性的で、一般論化され原理はないのが現状である。
我々は上記①~④に分類されないポリ(2-メトキシエチルアクリレート)(PMEA)がポリ(2-ヒドロキシエチルメタクリレート)(PHEMA)をはじめ、他の高分子に比べ、血漿蛋白の吸着が少なく血液適合性に優れる事を明らかにしている。それではこれらの特性が何によってもたらされているか?これが我々の現在の研究対象の1つである。
血液が材料と接触すると、先ずその表面へ水が吸着し、次いで血漿蛋白が吸着する。この吸着蛋白が変性した場合、これにより生体防御系の活性化が惹起されると考えられている。近年血液適合性発現において蛋白等が持つ結合水と材料表面の結合水の相互作用が重要な役割を果していると指摘され始めているが、依然、明確な水の構造は提案されていない。PMEAの血液適合性発現の機構を考えるに当たって我々もこの水の構造に着目し、示差走査熱量計(DSC)を用いて、PMEA、PHEMA、及びその共重合体、類似ポリマーについて血液適合性とポリマー中の水の構造*について比較考察を行った。その結果、PMEAを初め血液適合性を発現する材料は0℃以下(-数10℃)で結晶化する特異な水(中間水)を有する事を見出した。一方、PHEMA等適合性に劣る材料では中間水の存在を認めなかった。これらの事から我々は中間水という具体的な水が血液適合性発現に寄与*していると考え、これを証明するため多方面から研究を押し進めている。具体的にはこれら材料/水の構造と生体防御系活性化との詳細検討結果と、DSC、核磁気共鳴、表面赤外分光、X線回折、誘電緩和、等種々の分析から得られる結果を合わせる事で水と血液適合性の関係を解明しようとしている。同時にそのような水の構造を与える高分子側の化学構造、高次構造を解明し、次世代生体適合性材料の分子設計技術を構築しようとするものである。尚、本研究の遂行に当っては当Lab単独ではなく、他大学、他研究機関の協力を得、進めている。
|
**補足説明**
【ポリマー中の水の構造】
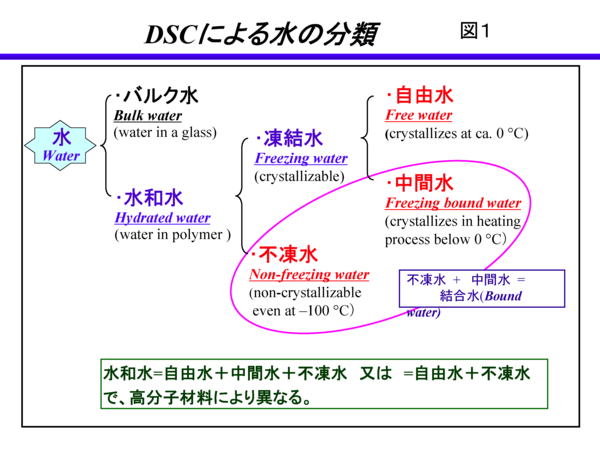
高分子材料は水をその中に取り込む。その取り込まれた水はコップの中の水(バルク水:0℃で凍る)とは異なった性質を有している。この水の分類定義は研究者により異なっているが、我々は現在、示差走査熱量分析(DSC)という手法により、図1のように、ポリマー中の水(水和水=Hydrated
Water)を3つに定義分けし、研究を進めている。この水和水は、まずは凍らない水(不凍水=Non-Freezing Water)と凍る水(凍結可能水=Freezing Water)とに二分される。不凍水は字の如くマイナス100℃に冷却しても凍らない水(高分子と強固な相互作用を有する水)であり、凍結可能水は0℃付近で凍る水(自由水=FreeWater:高分子との相互作用が非常に小さい)と、マイナス数十度で凍る水(中間水=Freezing BoundWater:高分子と中程度の相互作用がある水)の2つに分類される。尚、ここで定義する中間水は、DSCにおいて冷却過程では凍らず、マイナス100℃から温度を上げて行く昇温過程においてマイナス数十℃で凍るというユニークな特徴を有する(図2)。核磁気共鳴(NMR)に基づく緩和時間の研究からこの中間水は、自由水ほど運動性は高くはないが、不凍水ほど束縛された水でもない、その中間的な運動性を有する水である事が示唆されている。高分子中の水に対し以上のように自由水、中間水、不凍水の3つに定義分けしているが、高分子は基本的に自由水と不凍水は有するが中間水を有する例はあまり多くない。
【中間水と生体適合性】
中間水の存在が何ゆえ血液適合性に大きな役割を演じるか。血液中には生体を防御する為の各種システムが存在する。液性システムとしては蛋白群からなる血液を凝固させる凝固系、体内に侵入した細菌等を攻撃する補体系、免疫系が存在する。又、細胞性システムとしては液性と同様、血液凝固に関与する血小板、細菌等の異物を攻撃排除する白血球が存在する。これらのタンパク、細胞は血液中では水和されることで安定化している。この安定化に関与している水は自由水とは異なる水と考えられている。血液が人工材料に接触すると、生体防御システムを構成する蛋白或いは細胞の安定水和構造が破壊され、蛋白においてはコンフォメーションが変化、細胞においては膜構造が変化し、結果とし防御系が活性化される。従って生体防御系を活性化させないためにはその水和構造を乱さない事が必須と考えられる。即ち、材料表面或いはその表面に存在する不凍水と防御系を構成するタンパク或いは細胞が直接接触する事を妨げる事ができれば防御系の活性化を抑制できる事になる。これらの考えを基にPMEAをはじめとした血液適合性材料においてこの役割を演じるのが中間水であると研究仮説を立てている。この想定メカニズムをビジュアル化したものが図3である。
|
2.ドラッグデリバリーシステム(DDS)
ドラッグデリバリーシステムとは薬剤を患部に必要量、必要時に投与するシステムである。多くの場合、局所的或いは全身的に薬剤を長時間に渡って必要量、ゆっくりと放出させるシステムを指し、高分子材料中に薬剤を包埋させたものが研究されている。我々は薬剤溶出型冠動脈ステント*に用いるDDSシステムの開発を目的として高分子材料中からの薬剤放出の速度の制御とその制御機構について研究を行っている。
着任2年目で2005年度において初の卒業研究生を受け入れた若い研究室のため、研究分野が限定されていますが、今後マンパワーの充実にあわせ、研究領域を拡張したいと考えています。
|
**補足説明**
【冠動脈ステント】
狭心症、心筋梗塞は冠動脈が狭くなり心筋への血液供給が十分できなくなる極めて重篤な病気であり、この治療法として血管内からこの狭窄部位を拡張し、元の状態に戻すと言う、いわゆる風船療法がバイパス手術と並び行われている。しかしながら一旦風船療法で拡張に成功しても時間がたつと狭窄が再び起きてしまうケースが多々有り、これを改善する為に金属のメッシュ状の筒(ステント)をこの拡張部に留置し、再狭窄を防ぐ方法が考案された。しかしながらこの方法によっても再狭窄の予防は完璧でない事が明らかとなり、その原因が血管壁の肥厚にある事が解明された。その解決策として肥厚を抑制する為の薬剤がステントから徐放されるいわゆるDrug Eluting Stent(DES)がここ数年、注目を浴びるようになった。このDESにおいてもまだ完成した技術ではなく、現在でも薬剤の選定、その担持法、放出制御等について多くの研究が進行している。
|


|


